Contenido
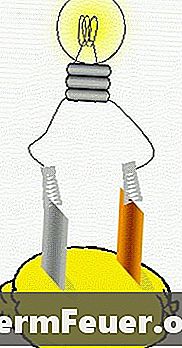
Batería de limón clásica (Theresa knott / wikicommons.org)
Construcción de la batería de limón
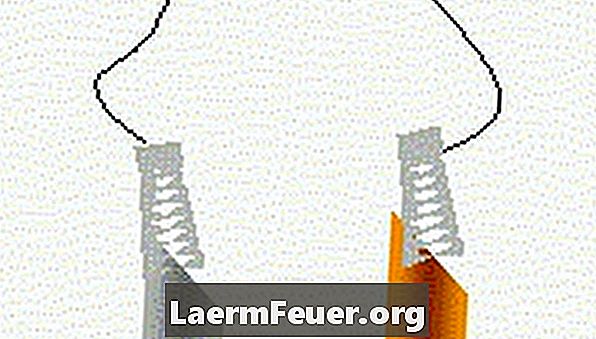
La batería de limón requiere una fruta ácida (limón), una moneda, un trozo de cinc (o un clip para papel de acero), dos hilos y un medidor de tensión. Dos hendiduras en el limón sujetan la moneda y el pedazo de cinc, con cada pieza envuelta en su propio hilo. Los extremos de estos hilos se conectan a un multímetro para medir el voltaje y la corriente eléctrica producidos por la batería de limón. Algunas experiencias conectan varios limones juntos, para entonces funcionar un reloj digital.
Qué pasa
El ácido del limón reacciona con los dos metales. El cobre y el acero (o cinc) actúan como electrodos en el ácido del limón. Los diversos metales permiten a los átomos de un metal moverse a través del limón hacia el otro metal. Este movimiento atómico no puede continuar indefinidamente, por lo que cuando, la batería muere. Conforme los átomos se mueven, ellos pierden electrones, que fluyen a través de los hilos, produciendo electricidad.
Producción de electricidad
La electricidad requiere un flujo de electrones. Las baterías de limón utilizan reacciones químicas para generar ese flujo de electrones. Esta conversión de energía química en eléctrica hace de la batería de limón una batería voltaica. La tensión generada a partir de un solo limón, normalmente, sólo registra 0,7 voltios. Para alimentar un reloj digital, se necesitan al menos dos baterías de limón conectadas en serie.